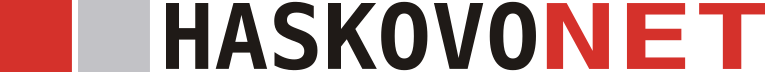Когато костта се счупи лошо – фрактура, твърде тежка, за да зарасне сама, или празнина, останала след отстраняване на тумор – хирурзите са изправени пред няколко несъвършени възможности. Те могат да вземат кост от друга част на тялото на пациента, болезнена процедура, която оставя траен дефект на донорското място. Те могат да използват метални или керамични импланти, които са механично здрави, но твърди и биологично инертни. Или могат да запълнят празнината с донорски костни парченца, които са подходящи за по-малки празнини, но не могат да възстановят големи сегменти.
„Няма нищо по отношение на лечението на голяма костна празнина, което да доведе до така нареченото биологично заздравяване“, което означава нова, жива, васкуларизирана кост, а не инертен пълнител, подчертава д-р Лукас Нистром (Lukas Nystrom), ортопедичен хирург в клиниката Кливланд, Кливланд.
Сега екип от Швейцарския федерален технологичен институт в Цюрих (ETH Zurich) е разработил потенциално решение, което изобщо не прилича на традиционен имплант: хидрогелно скеле, изработено от 97% вода и само 3% полимер, което може да бъде отпечатано с лазер в структури, достатъчно фини, за да имитират микроскопичната архитектура на костта. В проучване, публикувано в Advanced Materials, изследователите показват, че костообразуващите клетки лесно колонизират скелето и започват да произвеждат колаген - ключов градивен елемент на естествената кост.
Мека конструкция
Идеята за използване на желатинов материал за ремонт на нещо толкова механично сложно като костта звучи нелогично. Но изследователите са се вдъхновили от начина, по който самият организъм се лекува.
„Биологията на заздравяването на костни фрактури винаги започва от много мек, всъщност подобен на хидрогел материал“, обяснява д-р Сяо-Хуа Цин (Xiao-Hua Qin), старши автор на изследването и инженер по биоматериали в ETH Цюрих, Швейцария.
Когато някой счупи кост, първото нещо, което произвежда организмът, е мек, пропусклив хематом - скеле, подобно на синина, което привлича имунни клетки, хранителни вещества и прекурсори (суровини) на нова кост. Едва по-късно тази мека матрица постепенно се минерализира в твърда кост.
Цин обяснява, че тази матрица следва закона на Волф, основен принцип в костната биология, според който костта, която носи тежест, става по-силна, а костта, която не носи тежест, атрофира. Според него, твърд метален имплант работи против този принцип, предпазвайки околната тъкан от механични натоварвания. Хидрогелът, за разлика от него, може да се деформира с 40%-50% при натиск, без да се счупи - нещо, което керамичният или титаниевият имплант не може да направи.
„Хидрогеловете имат много сходни свойства по отношение на извънклетъчната матрица на нашия организъм и всъщност е прекурсор на развиващите се кости“, отбелязва д-р Даниел Беноа (Danielle Benoit), изследовател на хидрогеловете и костна регенерация в Университета на Орегон, Юджийн, Орегон, която не е участвала в проучването.
Тя посочва, че дори периостеумът – тънката тъкан, обграждаща костта, която е от решаващо значение за заздравяването – е по същество хидрогел в естественото си състояние.

Когато лазерът (червен лъч) удари молекулата на омрежващия агент (белезникава), той се свързва с околните полимерни нишки (оранжева). Кредит: Sven Gautschi/ETH ZurichКогато лазерът (червен лъч) удари молекулата на омрежващия агент (белезникава), той се свързва с околните полимерни нишки (оранжева). Кредит: Sven Gautschi/ETH Zurich
Химичният проблем е решен
Екипът използва техника, наречена двуфотонна полимеризация, при която силно фокусиран лазер се изстрелва в течен хидрогел, втвърдявайки само малката точка, където се събира лъчът - оставяйки всичко останало недокоснато. Чрез насочване на лъча през материала, изследователите могат да „пишат“ сложни триизмерни структури с детайли с размери до 500 nm (5 десетохилядни от милиметъра).
Предишни подходи, използващи тази техника, са изисквали високи концентрации на полимери – често 20%-50% – за постигане на добра прецизност на отпечатъка, което е водело до по-твърди гелове, които не имитират ранната костна тъкан. Проблемът бе в химията на омрежването, обяснява Цин.
Екипът на Цин е разработил нова свързваща молекула - макромолекулен тиол, който е по-голяма и по-здрава версия на късоверижните съединения, използвани от други лаборатории - която може да понесе множество реактивни места, като същевременно остава стабилна във вода.
Синтезът на полимери с множество тиолови групи не е бил лесен - химичният състав е трябвало да е точно такъв, че да се получат стабилни, водоразтворими молекули, които все пак могат да реагират ефективно под лазерна светлина.
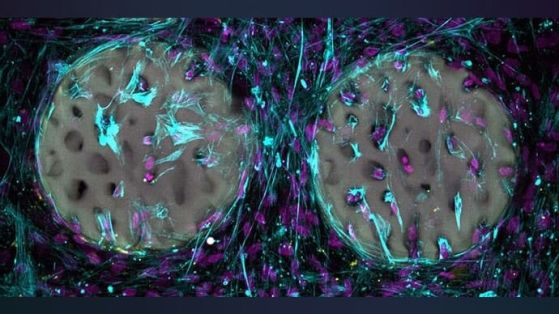
Костнообразуващите клетки (лилаво) са колонизирали костна структура на хидрогелна основа и произвеждат колаген (светлосиньо). Кредит: Xiao-Shua Qin / ETH Zurich
Резултатът е сложна хидрогелна структура, отпечатана със скорост на сканиране до 400 мм/сек, при само 3% концентрация на полимер. Беноа го нарича „наистина завладяващо“, отбелязвайки, че ниското съдържание на полимер и високата прецизност заедно представляват значителен напредък. Тя добавя, че макромолекулните системи за омрежване са, според нея, „със сигурност по-мощни“ от подходите с малки молекули, предлагайки по-голям потенциал за заздравяване.
Да накараме костните клетки да се чувстват като у дома си
Тъй като хидрогелът е синтетичен, клетките не взаимодействат естествено с него. За да преодолеят това, екипът функционализира скелета с къса пептидна последователност (RGD), която имитира фибронектин, протеин, който тялото използва за контрол на клетъчната адхезия. С тази модификация, костообразуващите клетки, наречени остеобласти, лесно колонизират отпечатаните структури и започват да отлагат колаген, без признаци на токсичност in vitro.
Идеята, казва Цин, е да се създаде имплант, който е „биологично поучителен“ – такъв, който не просто запълва празнина и се надява на най-доброто, а активно насочва клетъчното поведение по контролиран начин. „Искаме дори този имплант да отчита как клетките ще взаимодействат със скелета, в идеалния случай по много контролиран начин“, коментира Цин.
Дългият път до операционната зала
Резултатите от in vitro са обещаващи, но тази работа е далеч от клинично приложение.
Нистром отбелязва, че нуждата от подобна технология е реална. „Ако това е стъпка към това, тя би била изключително важна."
„Ако има решение, което е способно да се справи със сегментни костни дефекти с потенциал за създаване на жизнеспособна, васкуларизирана, нормална костна тъкан, това би било огромен скок напред в нашата област“, подчертава Цин.
Но изследователят отбелязва, че не е ясно дали този конкретен хидрогел може да се справи с такъв дефект въз основа на настоящите данни.
Беноа подчертава, че критичната следваща стъпка е преминаването към моделни животни.
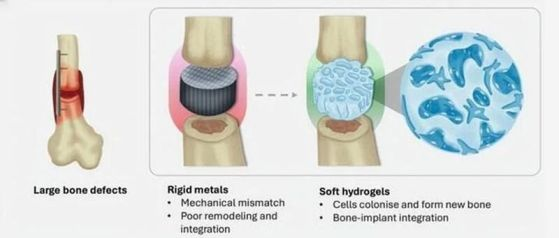
Метал срещу хидрогел: Сравнение. Кредит: Xiao-Shua Qin / ETH Zurich
Д-р Даниел Беноа очертава какво трябва да търсят изследователите в предклиничните изследвания: васкуларизация на импланта, минерализация, отлагане на тъкани, които са предшественици на зряла кост, и дали тези тъкани се превръщат по подходящ начин в костна тъкан. И преди всичко това, един по-основен въпрос: „Има ли сериозен възпалителен отговор, който ще попречи на заздравяването?"
Цин и колегите му сега си сътрудничат с Изследователския институт AO в Давос, за да започнат проучвания върху животни. Неговата дългосрочна визия е персонализирани импланти: интегриране на технологията за печат с медицинското изобразяване, така че да може да се изработи хидрогелно скеле, което да съответства на точната геометрия на нараняването на пациента. Различните пациенти – по-възрастни срещу по-млади, хронично болни срещу здрави – може да се нуждаят от различни биологични подобрения, потенциално включително утвърдени терапевтични средства като костен морфогенетичен протеин 2.
Безклетъчните подходи за костно заздравяване може да са на първо място
Един по-широк въпрос, висящ над темата, е дали хидрогелните импланти в крайна сметка ще трябва да бъдат засети с живи клетки преди имплантиране или дали безклетъчните скелета, които набират собствените клетки на тялото, могат да бъдат достатъчно ефективни.
Беноа казва, че клетъчната терапия е изправена пред значителни регулаторни пречки, свързани с вариабилността между пациентите, тестването на ефикасността и възпроизводимостта. Безклетъчните подходи заобикалят много от тези предизвикателства.
„Мисля, че вероятно първо ще видим повече безклетъчни подходи на пазара“, коментира тя, поради производството, логистиката и регулациите. Но тя признава компромиса: „Ако нямате стабилно набиране на клетки, няма да получите регенерация и може да се окажете с фиброзна тъкан, която е по-лоша от необходимата зряла тъкан."
Засега хидрогелът на ETH Zürich остава лабораторно постижение, което все още трябва да се докаже в жива кост. Но за област, където, както се изрази Нистром, „нищо смислено“ не се е променило в лечението на сегментни костни дефекти, стъпка в тази посока е от значение.
„Всичко, което ще работи вместо автотрансплантация, мисля, че ще бъде чудесно“, казва Цин.
Справка: Qiu W, Bernero M, Ye ME, Yang X, Fisch P, Müller R, Qin XH: A Water-Soluble PVA Macrothiol Enables Two-Photon Microfabrication of Cell-Interactive Hydrogel Structures at 400 mm s−1. Advanced Materials 2026: e10834, DOI: external page 10.1002/adma.202510834
Източник: New Hydrogel Helps Bone Grow Without Transplant or Implants Christina Szalinski, Medscape